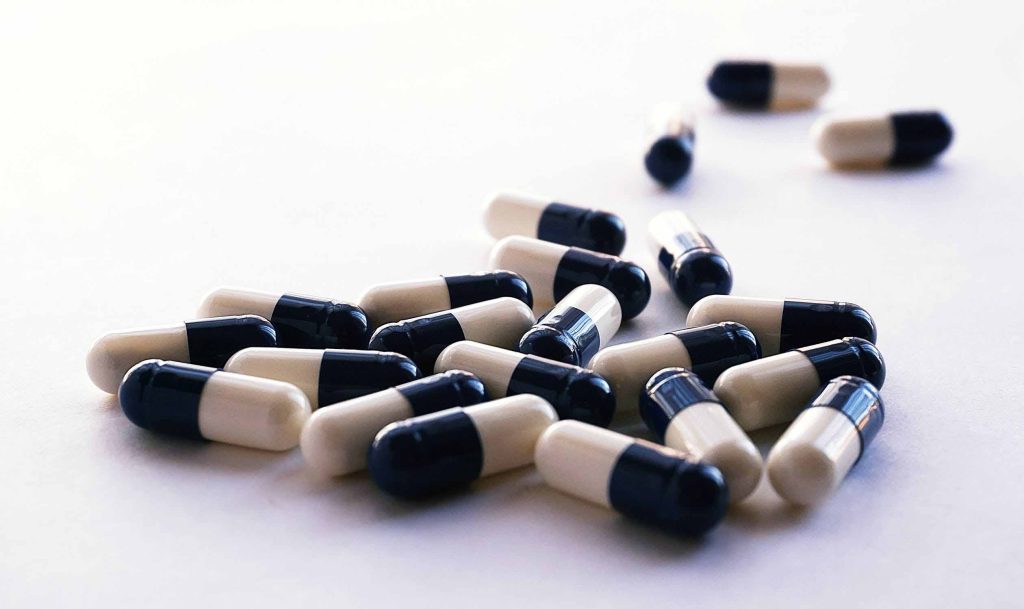
早期临床试验的发现可能指向一种生物标记物,该生物标记物可识别晚期非小细胞肺癌患者最有可能对免疫治疗药物彭布罗利珠单抗(Keytruda?)产生反应。扩大
染色片显示非小细胞肺癌PD-L1表达范围。图片由Dako North American,Inc.提供。早期临床试验中的
发现可能指向一种生物标记物,该生物标记物可识别最有可能对免疫治疗药物pembrolizumab(Keytruda?)产生反应的晚期非小细胞肺癌患者。试验中的
患者的肿瘤表达高水平的根据一项早期临床试验的结果,与肿瘤中PD-L1表达较低的患者相比,pembrolizumab治疗后PD-L1蛋白更可能在肿瘤中大量减少。这些患者在没有癌症进展的情况下也能活得更长。
这些试验结果在美国癌症研究协会(AACR)年会上发表,并同时发表在新英格兰医学杂志上。
被称为Keynote-001,这项试验最初是为了测试不同剂量的培溴利珠单抗的安全性和有效性,培溴利珠单抗是一种新兴的基于免疫的癌症治疗方法,被称为检查点抑制剂。但它在早期也被改变,以测试通过研究性免疫组织化学测试所测量的PD-L1表达水平是否能识别出最有可能对治疗产生反应的患者。
彭布罗珠单抗靶向免疫细胞上的一种蛋白质,称为PD-1,是一种所谓的检查点蛋白家族,它起作用,在很大程度上,抑制免疫反应。当肿瘤细胞上的PD-1配体或PD-L1与免疫系统细胞上的PD-1结合时,PD-1信号通路被激活,抑制免疫反应。通过阻断这种相互作用,彭布罗珠单抗使免疫系统能够识别和攻击肿瘤细胞。它已经被FDA批准用于治疗一些晚期黑色素瘤患者。
在AACR会议上展示的结果包括来自182名患者的培训,以确定PD-L1表达水平的临界点,这些水平似乎与肿瘤反应相关,以及一个由313名患者组成的独立验证集,以确认在训练集中选择的切点预测患者反应。
基于多个因素,选择的切点是在至少50%的样本肿瘤细胞中存在PD-L1表达,该研究的主要研究者爱德华·加龙医学博士解释说。,来自加州大学洛杉矶分校琼森综合癌症中心的
在验证集的73名患者中,其肿瘤具有这种水平的PD-L1表达,他报告说,肿瘤应答率为45.2%。在PD-L1水平超过这个临界点的试验中,所有患者的中位无进展生存期是6.3个月,他们的中位总生存期还没有达到,在验证集中,PD-L1阳性的肿瘤细胞比例为1-49%的患者(103例)和PD-L1阳性的肿瘤细胞比例小于1%的患者(137例)的应答率分别为16.5%和10.7%。加龙博士在一次新闻发布会上指出,这两组患者的无进展中位生存期和总生存期分别为3.3个月和8.8个月,以及2.3个月和8.8个月。最常见的副作用是疲劳。
“令人印象深刻的是,这项试验似乎能确定一组延长了[无进展生存期],”科罗拉多大学的Ross Camidge博士在AACR全体会议上介绍了研究结果后说,
“但这不是一项完美的试验,”他说警告。他说,许多患者,包括高PD-L1表达的患者,尽管接受了培溴利珠单抗治疗,但他们的疾病仍有快速进展,一些低PD-L1表达的患者也有反应。
,但不完善的[患者]富集策略仍能推动该领域向前发展,“卡米奇博士说,”
默克公司已经启动了几项随机临床试验来比较加龙博士说,彭布罗利珠单抗联合标准化疗治疗晚期肺癌,包括一项试验,纳入先前未经治疗的肿瘤细胞具有高PD-L1表达的患者。
进一步阅读
FDA批准肺癌的首次免疫治疗
治疗非小细胞肺癌